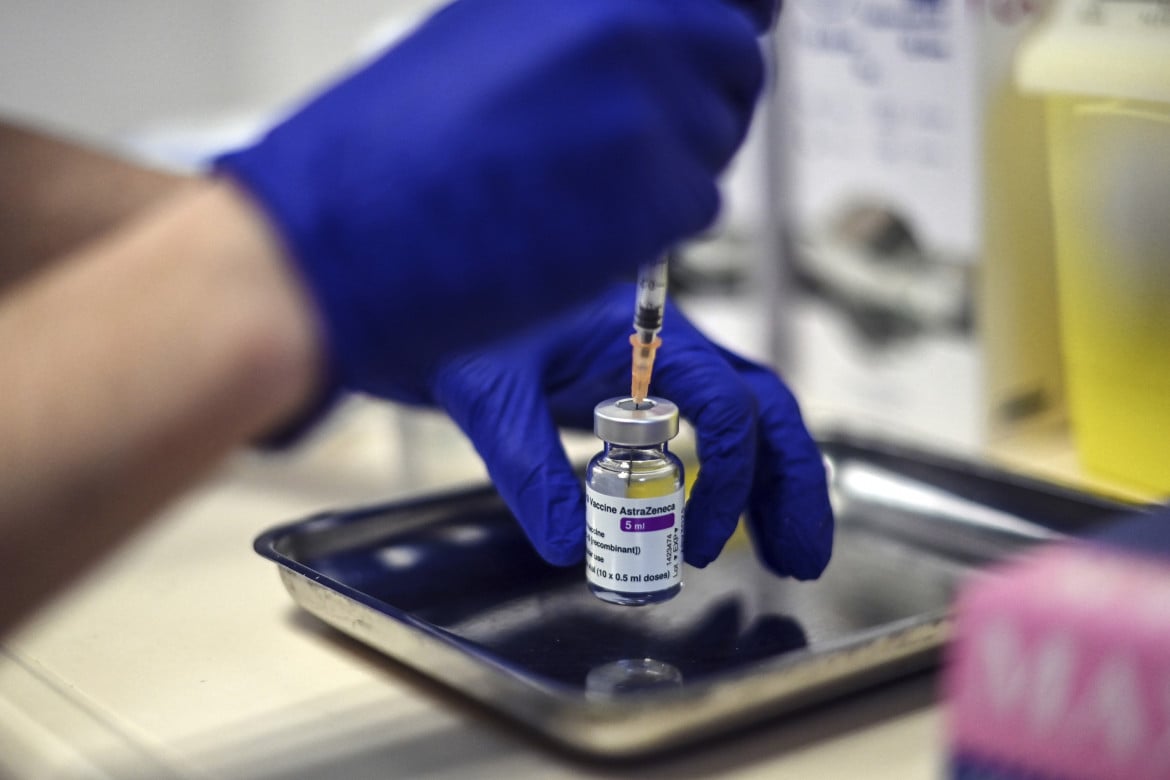
Anche chi ha più di 55 anni potrà ricevere il vaccino sviluppato dall’università di Oxford e prodotto dalla casa farmaceutica AstraZeneca. Ma per l’ok definitivo è necessario un ulteriore parere da parte della Commissione tecnico scientifica dell’Agenzia del farmaco (Aifa). Il nuovo parere di Aifa dovrebbe alzare il limite per la somministrazione del vaccino fino ai 65 anni di età.
La riunione di ieri tra gli esperti del ministero della salute, vertici dell’Agenzia del farmaco (Aifa) e regioni, dunque, non è bastata. Il ministero ha chiesto che si esprima la Commissione Tecnico Scientifica dell’Aifa, convocata nei prossimi giorni. Il parere favorevole dell’Aifa è scontato e non è nemmeno strettamente necessario. In un precedente parere la commissione aveva già valutato la somministrazione negli anziani del vaccino AstraZeneca senza escluderla del tutto. Il parere aveva raccomandato «un utilizzo preferenziale» nei soggetti di età compresa tra i 18 e i 55 anni, ma aggiungeva che «il rapporto beneficio/rischio di tale vaccino risulta favorevole anche nei soggetti di età più avanzata che non presentino specifici fattori di rischio».
I dubbi dell’Aifa nascono dalle scarse conoscenze sull’efficacia del vaccino nelle fasce di età più avanzata. Secondo gli esperti dell’Aifa, i dati «mostrano un livello di incertezza nella stima di efficacia» al di sopra dei 55 anni, perché agli studi clinici hanno partecipato pochi volontari anziani. Tuttavia, studi precedenti avevano dimostrato che anche al di sopra dei 55 anni la vaccinazione stimola la produzione di un numero notevole di anticorpi. Dal punto di vista della sicurezza, inoltre, ci sono poche controindicazioni.
Nemmeno le agenzie internazionali, d’altronde, si oppongono all’uso del vaccino nei soggetti più anziani. L’autorizzazione al commercio dell’Agenzia Europea del farmaco, che ha preceduto quello nazionale, si limita a specificare che il vaccino è autorizzato «in persone al di sopra dei 18 anni di età», senza limiti massimi. La stessa raccomandazione è stata adottata dall’Organizzazione Mondiale della Sanità.
Grazie all’allargamento della platea delle persone da immunizzare con il vaccino inglese, la campagna di vaccinazione dovrebbe accelerare, dosi permettendo. Il vaccino AstraZeneca, infatti, è più maneggevole rispetto a quelli della Moderna e della Pfizer, perché non richiede una conservazione a temperature particolarmente basse. Perciò, anche i circa 50 mila medici di famiglia potranno presto somministrarlo al personale scolastico, alle forze dell’ordine, ai detenuti e alla polizia penitenziaria.
Allargare la platea permetterà di vaccinare per intero le categorie individuate. Con il limite a 55 anni, invece, solo i lavoratori più giovani sarebbero stati tutelati. Nella scuola, dove l’età media tra i docenti è proprio di 55 anni di età, la metà del personale più a rischio avrebbe rischiato di rimanere senza copertura. Per questo diversi amministratori, come l’assessore alla sanità del Lazio Alessio D’Amato, chiedono da giorni di alzare la soglia di età: «è necessario non spaccare le categorie lavorative, si crea un discrimine e si rallenta la copertura», ha detto D’Amato.
Ma non tutti sono felici per l’estensione del piano. Dato che il vaccino AstraZeneca offre una protezione del 60% circa, contro il 90-95% dei vaccini Moderna e Pfizer, alcune categorie avrebbero preferito aspettare la disponibilità del vaccino più efficace. Quello di AstraZeneca «è un vaccino non adatto a noi – sostiene Paolo Mezzana, portavoce di tremila medici e odontoiatri riuniti in gruppo su Facebook – perché l’immunità si raggiunge in un periodo troppo lungo rispetto ai vaccini ad mRna. E questo non va bene, per personale che deve garantire la medicina sul territorio».
Un ulteriore aiuto al piano vaccinale potrebbe arrivare dal nuovo vaccino della Johnson & Johnson, che proprio ieri ha presentato la richiesta di autorizzazione all’Ema. Nei test ha mostrato un’efficacia non elevatissima, compresa tra il 72% negli Usa e il 57% in Sudafrica (forse a causa delle varianti). Ma ha il vantaggio di richiedere un’unica dose. La decisione dell’Ema arriverà entro la metà di marzo e i 200 milioni di dosi prenotati dall’Europa potrebbero essere distribuiti a partire dal mese di aprile.